
Captage du CO2 et chimie du carbone inorganique (Cinorg) dans l'eau sont deux sujets à toutes fins pratiques indissociables et sont traités ici ensemble.
Un premier niveau de captage du CO2 qui agit sur terre et dans l'océan est celui de la photosynthèse qui transforme le Cinorg du CO2 en Corg et qui s'exprime par l'équation suivante:

Un second niveau très important est la dissolution du CO2 dans l'océan. Quand le CO2 est dissout dans l'eau, qu'elle soit douce (terrestre) ou salée (océans), de l'acide carbonique se forme:

Cet acide carbonique se dissocie en libérant ses atomes d'hydrogène. Quand son premier atome est libéré, il se forme un ion bicarbonate:
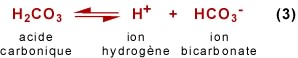
Le pH de l'eau contrôle cette réaction. Si la concentration en H+ diminue, ce qui correspond à une augmentation de pH, le rééquilibrage de l'équation entraîne une réaction vers la droite et une plus grande quantité d'acide carbonique se dissocie. À l'inverse, une augmentation de la concentration en H+ (soit une diminution du pH) entraîne une réaction vers la gauche et forme H2CO3 au détriment de HCO3-.
Quand le second atome d'hydrogène de l'acide carbonique est libéré, le bicarbonate HCO3- se transforme en carbonate CO32- selon:
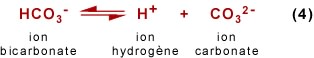
Pour une concentration en H+ donnée, c'est-à-dire à un pH de l'eau donné, les quantités relatives d'ions carbonates et bicarbonates s'ajustent jusqu'à l'atteinte de l'équilibre. Un pH supérieur à 7 (on se rapellera que 7 est le pH neutre), favorise la production des ions carbonates, alors qu'un pH inférieur à 7 favorise les ions bicarbonates. De manière générale, les eaux marines sont alcalines (pH > 7) et les eaux douces continentales sont acides (pH < 7).
La perturbation de cet équilibre, par exemple par la diffusion de CO2 anthropique de l'atmosphère vers l'océan, changera le pH de l'eau marine. Un changement de pH affectera les concentrations relatives de l'acide carbonique H2CO3, des ions bicarbonates HCO3- et des ions carbonates CO32- de la façon suivante: la dissolution du CO2 forme de l'acide carbonique (réaction 2), et la dissociation de l'acide carbonique produit des ions bicarbonates et hydrogènes (réaction 3), la production de ces derniers entraînant un abaissement de pH. Les ions hydrogènes réagissent alors avec les ions carbonates pour former d'autres ions bicarbonates (inverse de la réaction 4, c'est-à-dire réaction vers la gauche). La réaction chimique exprimant le captage d'un excès de CO2 par l'océan est la somme de ces trois réactions, soit:
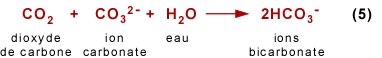
Ainsi, à cause du fait qu'il y a conversion du carbone du CO2 en d'autres formes de carbone, la capacité de l'océan à capter un excès de CO2 atmosphérique (par exemple, anthropique) est augmentée par rapport à ce qu'elle serait s'il n'y avait qu'un simple équilibre des pressions entre atmosphère et océan. Mais, il y a une limite à cette capacité. Ce sont les ions carbonates CO32- qui tamponnent le pH de l'eau marine et c'est leur quantité qui fixera la limite. À cet égard, deux choses sont à considérer par rapport à la production de CO2 atmosphérique issue de la combustion des pétroles et des charbons: 1) la capacité de tamponnage de l'océan superficiel (de 0 à 100 mètres de profondeur) est très faible; 2) on évalue que l'océan intermédiaire et profond (de 100 à 4000 mètres) contient une quantité d'ions carbonates pour tamponner au plus 30% du réservoir actuel des combustibles fossiles. La conclusion n’est pas des plus difficiles à tirer!
Une chimie semblable à celle des eaux océaniques s'applique à la dissolution du CO2 dans les eaux de pluies (réactions 2 et 3), les rendant naturellement acides (pH normalement entre 5 et 6, quand il n'est pas encore plus faible à cause de la pollution). Ces eaux acides viennent altérer chimiquement les massifs rocheux continentaux. Les produits de cette altération, une fois transférés dans le bassin océanique par les cours d'eau, ont une influence sur la capacité de captage du CO2 des océans.
L'altération chimique des deux grands types de minéraux, les silicates et les carbonates (voir au point 2.1.4 les minéraux constitutifs de l’écorce terrestre), est particulièrement significative. Un des produits d'altération important ici est l'ion calcium Ca2+. Ce calcium est abondant chez les carbonates dont les deux principaux minéraux sont la calcite CaCO3 (carbonate de calcium) et la dolomite CaMg(CO3)2 (carbonate de calcium et magnésium). Chez les silicates, on trouve du calcium dans des minéraux comme les feldspaths plagioclases (Na,Ca)AlSi3O8 ou les amphiboles comme la hornblende NaCa2(Mg,Fe,Al) 5(Si,Al)8O22 (OH)2. Pour simplifier les écritures chimiques, nous allons utiliser la wollastonite CaSiO3 pour représenter les silicates de calcium.
Lorsque soumis aux pluies (acides), ces deux groupes de minéraux se dissolvent, les carbonates étant de loin les plus rapidement attaqués. Dans les deux cas, des ions calcium et bicarbonates sont produits:

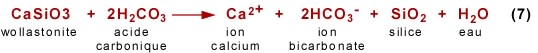
Chez les deux processus d'altération, des ions calcium Ca2+ et bicarbonates HCO3- sont produits. Dans le cas des silicates calciques, l'altération produit en sus de la silice. Calcium, bicarbonate et silice sont arrachés aux sols par l'érosion et transportés vers l'océan par les cours d'eau. Ces trois produits viennent contribuer à la charge sédimentaire des océans. Certains organismes comme les diatomées, les radiolaires et les éponges utilisent la silice dissoute dans l'eau de mer pour secréter leur squelette. Le gros des ions Ca2+ et HCO3- est utilisé par la plupart des autres organismes marins à squelette minéralisé pour secréter un squelette ou une coquille de carbonate de calcium (CaCO3, calcite ou aragonite); une autre partie des ions Ca2+ et HCO3-, vient former abiotiquement du CaCO3, mais en volume beaucoup plus faible par rapport à celui des squelettes des organismes. Cette précipitation du carbonate de calcium, qu'elle soit biotiquement ou abiotiquement contrôlée, vient soustraire à l'eau marine des ions Ca2+ et HCO3- selon la réaction inverse de la réaction 6:

Cette production de CaCO3 modifie la chimie du carbone des océans en entraînant deux choses: 1) une augmentation de la concentration en acide carbonique (H2CO3 qui peut aussi s'écrire CO2 + H2O, selon l'équation 1) et, par voie de conséquence, de celle du CO2; 2) une réduction de la concentration en ions bicarbonates, ce qui signifie un abaissement du pH. L'augmentation de la concentration en CO2 reliée à cette production de CaCO3 entraîne la création d'un gradient entre l'océan et l'atmosphère qui favorise une diffusion du CO2 de l'océan vers l'atmosphère.
En somme, on peut dire qu'une accélération de l'altération des carbonates et des silicates continentaux (par exemple, par des pluies rendues plus acides par la pollution) aura pour conséquence une augmentation de la production océanique de CaCO3, qui entraînera une augmentation de la pression partielle de CO2 dans l'eau de mer, qui entraînera à son tour une plus grande diffusion de CO2 dans l'atmosphère à partir de l'océan, ce qui vient modérer cette capacité de l'océan à capter un excès de CO2 atmosphérique dont on a discuté plus haut (réactions 2 à 5).
La modélisation n'est pas des plus simples, n'est-ce pas?
